急性心肌梗塞患者红细胞左旋精氨酸—一氧化氮途径的变化
作者:王晓阳 丁文惠 李建平 王晓红 姚兴海 唐朝枢
单位:王晓阳 丁文惠 李建平(10 0034 北京市,北京医科大学第一医院 心内科);王晓红 姚兴海 唐朝枢(心血管研究所)
关键词:心肌梗塞;一氧化氮;红细胞
中国循环杂志000206 摘要
目的:探讨急性心肌梗塞患者红细胞左旋精氨酸—一氧化氮(L-Arg-NO)途径变化及临床意义。
方法:14例急性心肌梗塞患者为急性心肌梗塞组,10例健康成人为正常对照组,取静脉抗凝血,分离并提纯红细胞,同位素标记法测定3H标记左旋精氨酸(3H-L-Arg)的转运动力学;分离纯化一氧化氮合酶(NOS)后测定其含量及活性;放射免疫法测定红细胞环磷酸鸟苷(cGMP)含量。
, 百拇医药
结果:急性心肌梗塞组患者红细胞①L-Arg的总转运及Y+载体的最大转运速率(Vmax)分别较正常对照组降低14%(P<0.05)及18%(P<0.01),米氏常数(Km)分别增加32%及46%(P<0.01);Y+L载体无改变。②NOS含量及活性分别较正常对照组降低13%(P<0.05)及44%(P<0.01)。③cGMP含量较正常对照组下降27%(P<0.05)。
结论:急性心肌梗塞患者红细胞L-Arg-NO途径存在多环节功能障碍,导致一氧化氮(NO)生成减少,可能会促进急性心肌梗塞的进展。
中图分类号:R542.2+2 文献标识码:A
文章编号:1000-614(2000)02-078-3
The Changes of L-Arginine-Nitric Oxide Pathway of Erythrocyte in
, 百拇医药
Patients with Acute Myocardial Infarction
Wang Xiaoyang,Ding Wenhui,Wang Xiaohong,et al.
Department of Cardiology,First Hospital,Beijing Medical University,Beijing(100034)
Abstract
Objective:To study the changes and the clinical significance of L-arginine-nitric oxide(L-Arg-NO)pathway of erythrocyte in patients with acute myocardial infarction(AMI).
, 百拇医药
Methods:Erythrocytes were isolated and washed from venous blood taken from 14 patients with AMI and 10 normal controls.3H-L-Arg transport was measured by radionuclide labeling,content and activity of NO synthase(NOS) were measured after being isolated and purified,content of cyclic guanosine 3,5-monophosphate(cGMP) was measured by radioimmunoassay.
Results:①Maximum transport velocity(Vmax) of total L-arg transport and that of system Y+ decreased 14% (p<0.05) and 18% (p<0.01) respectively,while Michaelis constant (Km) increased 32% and 46%(p<0.01) respectively in AMI patients than those in controls.No significant difference of system Y+L was found between two groups.②The content and activity of NOS decreased 13% (p<0.05) and 44% (p<0.01) respectively in AMI patients than those in controls.③The cGMP content of erythrocytes in AMI patients decreased 27% than that in controls (p<0.05).
, 百拇医药
Conclusion:An abnormal function of L-Arg-NO pathway of erythrocytes was found in AMI patients which would decrease the production of NO and exacerbate the disease.
Key words Myocardial infarction;Nitric oxide;Erythrocyte
(Chinese Circulation Journal,2000,15:78.)
冠状动脉内血栓形成是急性心肌梗塞的主要原因,而内皮或血小板功能障碍导致一氧化氮(NO)生成减少可促进血栓形成[1]。近年发现红细胞也存在左旋精氨酸—一氧化氮(L-Arg-NO)途径,并参与了血管舒缩和血小板粘附、聚集功能的调节[2]。但急性心肌梗塞时红细胞L-Arg-NO途径是否有变化尚未见报道。本工作通过测定急性心肌梗塞患者红细胞L-Arg转运动力学、一氧化氮合酶(NOS)含量和活性以及环磷酸鸟苷(cGMP)生成量,探讨其L-Arg-NO途径变化及临床意义。
, 百拇医药
1 资料和方法
病例选择及分组 ①急性心肌梗塞组:14例,选自1998年10月~11月收入我院冠心病监护室的住院患者,男10例,女4例,平均年龄(57±10)岁,均符合世界卫生组织急性心肌梗塞的诊断标准,胸痛至入院时间为5.1±2.2小时。其中前壁梗塞10例,下、后壁梗塞4例;心功能均为Killip 1级。②正常对照组:健康成人10例,其中男7例,女3例,平均年龄54±8岁。
红细胞采集及制备 急性心肌梗塞组患者入院即刻、正常对照组晨8时取静脉抗凝血4 ml,按照红细胞采集及制备方法分离并提纯红细胞[3]。
红细胞L-Arg转运[4,5] ①首先使红细胞达到零转运状态。②红细胞悬液中加入N-ethylmaleimide(NEM)抑制Y+载体,孵育15分后加终止液。③3H标记左旋精氨酸(3H-L-Arg)转运实验:各取1 ml红细胞悬液(1×107 cells/ml)分别加入浓度为5~400 μmol/L的3H-L-Arg,温育5分后,冲洗、融解细胞,β液闪计数仪测定放射活性。经NEM处理的3H-L-Arg转运由Y+L系统介导,未经处理的总转运减去Y+L介导的转运则为Y+介导的转运。
, 百拇医药
红细胞NOS活性测定[6] 将红细胞(5×107 cells)冻融,按NOS提纯方法分离[3]、纯化NOS,蛋白浓度用Bradford Method测定。取20 μg提纯的NOS,加入2 Ci 3H-L-Arg及还原型辅酶Ⅱ(NADPH)、氯化钙等。孵育15分,加终止液,过Dowex AG 50WX-8柱。β液闪方法测3H放射活性。NOS活性以每毫克NOS每分生成的3H-瓜氨酸表示。
红细胞cGMP含量测定[6] 红细胞悬液与0.1 mmol/L L-Arg孵育30分,离心,去上清液,加入乙醇,真空离心,红细胞悬浮于3羟甲基氨基甲烷/依地酸(Tris/EDTA)缓冲液中,振荡10分,离心,取上清液用放射免疫法测cGMP含量,以pmol/5×107 RBC表示。
材料 L-(2,3-3H) Arg (53 Ci/mmol)购自Amersham,cGMP药盒购自上海中医药大学,其它试剂均购自美国Sigma公司。
, 百拇医药
统计学方法 结果以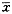 ±s表示,组间资料用t检验进行统计学处理。
±s表示,组间资料用t检验进行统计学处理。
2 结果
急性心肌梗塞对红细胞3H-L-Arg转运的影响:红细胞L-Arg主要由Y+载体转运,少量由Y+L载体转运。急性心肌梗塞组的总转运速率在不同浓度底物L-Arg时均较正常对照组降低(P<0.01),其中主要为Y+载体转运速率下降(P<0.01),而Y+L载体在正常对照组及急性心肌梗塞组均无明显变化(P>0.05,附图)。Eadie-Hofstee Plot分析:两组的总转运、Y+转运、Y+L转运均呈高亲和特征。急性心肌梗塞组总转运及Y+载体的最大转运速率(Vmax)分别较正常对照组降低14%(P<0.05)及18%(P<0.01),米氏常数(Km)增加32%及46%(P<0.01),而Y+L载体的Vmax及Km与正常对照组差异无显著性(P>0.05,表1)。
, 百拇医药
附图 急性心肌梗塞组和正常对照组红细胞左旋精氨酸转运饱和曲线
表1 2组患者红细胞左旋精氨酸最大转运速率和米氏常数比较(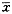 ±s) 组别
±s) 组别
例数
最大转运速率[nmol/(107 cells.min)]
米氏常数(μmol/L)
总内流
Y+载体
Y+L载体
, 百拇医药
总内流
Y+载体
Y+L载体
正常对照组
10
5.27±0.40
4.35±0.32
0.98±0.06
31.7±4.0
33.3±2.9
27.7±3.3
急性心肌梗塞组
, http://www.100md.com
14
4.52±0.32*
3.58±0.26**
0.97±0.06
41.8±3.2**
48.5±4.2**
26.9±2.6
注:与正常对照组比*P<0.05 **P<0.01
急性心肌梗塞对红细胞NOS含量、NOS活性及cGMP含量的影响:急性心肌梗塞组患者红细胞NOS含量及NOS活性分别较正常对照组降低13%(P<0.05)及44%(P<0.01);cGMP含量较正常对照组下降27%(P<0.05,表2)。
, 百拇医药
表2 2组患者红细胞内一氧化氮合酶含量、活性及环磷酸鸟苷含量比较(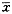 ±s) 组别
±s) 组别
例数
一氧化氮合酶含量
(mg/5×107 cells)
一氧化氮合酶活性
(pmol/mg.min)
环磷酸鸟苷含量
(pmol/5×107 RBC)
正常对照组
, 百拇医药
10
0.52±0.06
22.51±3.26
0.22±0.02
急性心肌梗塞组
14
0.45±0.03*
12.71±2.21**
0.16±0.02*
注:与正常对照组比*P<0.05 **P<0.01
, 百拇医药
3 讨论
急性心肌梗塞主要病因是冠状动脉内血栓形成,已知内皮及血小板NO生成减少可促进血栓形成,可能是急性心肌梗塞的发病环节之一[1]。近年发现不仅血小板和内皮细胞中存在L-Arg-NO途径,红细胞也存在L-Arg-NO途径:即血浆中的NO合成的底物L-Arg经Na+—非依赖性高亲和Y+载体和Y+L载体转运入红细胞[4],在红细胞内存在的内皮型一氧化氮合酶(eNOS)作用下,生成NO,并持续、小量地释放入血,通过细胞的第二信使cGMP发生抑制血小板凝集、调节血管张力、减轻缺血再灌注损伤等心血管保护作用[2]。但急性心肌梗塞时红细胞L-Arg-NO途径是否发生变化尚未见报道。
本工作观察到红细胞L-Arg的跨膜转运主要由Y+载体介导,少量由Y+L载体介导,与文献报道一致[4]。急性心肌梗塞时转运方式无改变,但Y+载体的Vmax较正常对照组降低,Km增加,提示参与转运的载体数量减少且与L-Arg的亲和力下降;而Y+L载体无明显变化。所以急性心肌梗塞时红细胞L-Arg的总转运能力是下降的。
, 百拇医药
除L-Arg的跨膜转运外,NOS是NO生成过程的另一重要限速步骤。本研究结果发现急性心肌梗塞患者红细胞内NOS含量及NOS活性均较正常对照组降低。cGMP是NO的下游分子,红细胞内cGMP的含量与内源性NO生成量一致[6],测定cGMP的含量可以间接反映NO的生成量。结果显示急性心肌梗塞组患者红细胞cGMP的含量较正常对照组下降,提示NO生成减少。NO的减少可增加血小板的高反应性,促进血栓形成,增加血管张力,可能会在一定程度上加速急性心肌梗塞的进程,加重心肌缺血—再灌注损伤,促进溶栓后血管再闭塞或再次心肌梗塞。
本研究结果表明,急性心肌梗塞患者红细胞存在L-Arg-NO途径的多环节功能障碍,最终使NO生成减少,可能会加重或促进血栓的形成,提示临床上需加强急性心肌梗塞后抗凝、抗血小板治疗;也支持应用硝酸酯类等NO供体,以迅速、有效地补充NO,不仅能扩张冠状动脉、增加冠状动脉血流,也能防止血小板粘附、聚集。由于L-Arg转运具饱和性质,补充L-Arg等NO前体时需考虑其生物利用度。急性心肌梗塞患者红细胞L-Arg-NO途径异常的发生机制尚不清楚,需进行深入研究。
, http://www.100md.com
作者简介:王晓阳(1965-)女,主治医师 硕士研究 生 主要从事心血管临床工作
参考文献
1,Freedman JE,Ting B,Hankin B,et al.Impaired platelet production of nitric oxide predicts presence of acute coronary syndromes.Circulation,1998,98:1481—1486.
2,Chen LY,Mehta JL.Evidence for the presence of L-arginine-nitric oxide pathway in human red blood cells:relevance in the effects of red blood cells on platelet function.J Cardiovasc Pharmacol,1998,32:57—61.
, 百拇医药
3,Deliconstantions G,Villiotou V,Stavrides JC,et al.Nitric oxide and peroxynitrite production by human erythrocytes:a causative factor of toxic anemia in breast cancer patients.Anticancer Res,1995,15:1435—1446.
4,Ribeiro ACM,Hanssen H,Kiessling K,et al.Transport of L-arginine and the nitric oxide inhibitor NG-monomethyl-L-arginine in human erythrocytes in chronic renal failure.Clin Sci,1997,93:57—64.
5,Deves R,Angelo S,Chavez P.N-Ethylmaleimide discriminates between two lysine transport systems in human erythrocytes.J Physiol,1993,468:753—766.
6,Ghigo D,Todde R,Ginsburg H,et al.Erythrocyte stages of Plasmodium falciparum exhibit a high nitric oxide synthase (NOS) activity and release an NOS-inducing soluble factor.J Exp Med,1995,182:677—688.
收稿:1999-09-06
修回:2000-01-26, 百拇医药
单位:王晓阳 丁文惠 李建平(10 0034 北京市,北京医科大学第一医院 心内科);王晓红 姚兴海 唐朝枢(心血管研究所)
关键词:心肌梗塞;一氧化氮;红细胞
中国循环杂志000206 摘要
目的:探讨急性心肌梗塞患者红细胞左旋精氨酸—一氧化氮(L-Arg-NO)途径变化及临床意义。
方法:14例急性心肌梗塞患者为急性心肌梗塞组,10例健康成人为正常对照组,取静脉抗凝血,分离并提纯红细胞,同位素标记法测定3H标记左旋精氨酸(3H-L-Arg)的转运动力学;分离纯化一氧化氮合酶(NOS)后测定其含量及活性;放射免疫法测定红细胞环磷酸鸟苷(cGMP)含量。
, 百拇医药
结果:急性心肌梗塞组患者红细胞①L-Arg的总转运及Y+载体的最大转运速率(Vmax)分别较正常对照组降低14%(P<0.05)及18%(P<0.01),米氏常数(Km)分别增加32%及46%(P<0.01);Y+L载体无改变。②NOS含量及活性分别较正常对照组降低13%(P<0.05)及44%(P<0.01)。③cGMP含量较正常对照组下降27%(P<0.05)。
结论:急性心肌梗塞患者红细胞L-Arg-NO途径存在多环节功能障碍,导致一氧化氮(NO)生成减少,可能会促进急性心肌梗塞的进展。
中图分类号:R542.2+2 文献标识码:A
文章编号:1000-614(2000)02-078-3
The Changes of L-Arginine-Nitric Oxide Pathway of Erythrocyte in
, 百拇医药
Patients with Acute Myocardial Infarction
Wang Xiaoyang,Ding Wenhui,Wang Xiaohong,et al.
Department of Cardiology,First Hospital,Beijing Medical University,Beijing(100034)
Abstract
Objective:To study the changes and the clinical significance of L-arginine-nitric oxide(L-Arg-NO)pathway of erythrocyte in patients with acute myocardial infarction(AMI).
, 百拇医药
Methods:Erythrocytes were isolated and washed from venous blood taken from 14 patients with AMI and 10 normal controls.3H-L-Arg transport was measured by radionuclide labeling,content and activity of NO synthase(NOS) were measured after being isolated and purified,content of cyclic guanosine 3,5-monophosphate(cGMP) was measured by radioimmunoassay.
Results:①Maximum transport velocity(Vmax) of total L-arg transport and that of system Y+ decreased 14% (p<0.05) and 18% (p<0.01) respectively,while Michaelis constant (Km) increased 32% and 46%(p<0.01) respectively in AMI patients than those in controls.No significant difference of system Y+L was found between two groups.②The content and activity of NOS decreased 13% (p<0.05) and 44% (p<0.01) respectively in AMI patients than those in controls.③The cGMP content of erythrocytes in AMI patients decreased 27% than that in controls (p<0.05).
, 百拇医药
Conclusion:An abnormal function of L-Arg-NO pathway of erythrocytes was found in AMI patients which would decrease the production of NO and exacerbate the disease.
Key words Myocardial infarction;Nitric oxide;Erythrocyte
(Chinese Circulation Journal,2000,15:78.)
冠状动脉内血栓形成是急性心肌梗塞的主要原因,而内皮或血小板功能障碍导致一氧化氮(NO)生成减少可促进血栓形成[1]。近年发现红细胞也存在左旋精氨酸—一氧化氮(L-Arg-NO)途径,并参与了血管舒缩和血小板粘附、聚集功能的调节[2]。但急性心肌梗塞时红细胞L-Arg-NO途径是否有变化尚未见报道。本工作通过测定急性心肌梗塞患者红细胞L-Arg转运动力学、一氧化氮合酶(NOS)含量和活性以及环磷酸鸟苷(cGMP)生成量,探讨其L-Arg-NO途径变化及临床意义。
, 百拇医药
1 资料和方法
病例选择及分组 ①急性心肌梗塞组:14例,选自1998年10月~11月收入我院冠心病监护室的住院患者,男10例,女4例,平均年龄(57±10)岁,均符合世界卫生组织急性心肌梗塞的诊断标准,胸痛至入院时间为5.1±2.2小时。其中前壁梗塞10例,下、后壁梗塞4例;心功能均为Killip 1级。②正常对照组:健康成人10例,其中男7例,女3例,平均年龄54±8岁。
红细胞采集及制备 急性心肌梗塞组患者入院即刻、正常对照组晨8时取静脉抗凝血4 ml,按照红细胞采集及制备方法分离并提纯红细胞[3]。
红细胞L-Arg转运[4,5] ①首先使红细胞达到零转运状态。②红细胞悬液中加入N-ethylmaleimide(NEM)抑制Y+载体,孵育15分后加终止液。③3H标记左旋精氨酸(3H-L-Arg)转运实验:各取1 ml红细胞悬液(1×107 cells/ml)分别加入浓度为5~400 μmol/L的3H-L-Arg,温育5分后,冲洗、融解细胞,β液闪计数仪测定放射活性。经NEM处理的3H-L-Arg转运由Y+L系统介导,未经处理的总转运减去Y+L介导的转运则为Y+介导的转运。
, 百拇医药
红细胞NOS活性测定[6] 将红细胞(5×107 cells)冻融,按NOS提纯方法分离[3]、纯化NOS,蛋白浓度用Bradford Method测定。取20 μg提纯的NOS,加入2 Ci 3H-L-Arg及还原型辅酶Ⅱ(NADPH)、氯化钙等。孵育15分,加终止液,过Dowex AG 50WX-8柱。β液闪方法测3H放射活性。NOS活性以每毫克NOS每分生成的3H-瓜氨酸表示。
红细胞cGMP含量测定[6] 红细胞悬液与0.1 mmol/L L-Arg孵育30分,离心,去上清液,加入乙醇,真空离心,红细胞悬浮于3羟甲基氨基甲烷/依地酸(Tris/EDTA)缓冲液中,振荡10分,离心,取上清液用放射免疫法测cGMP含量,以pmol/5×107 RBC表示。
材料 L-(2,3-3H) Arg (53 Ci/mmol)购自Amersham,cGMP药盒购自上海中医药大学,其它试剂均购自美国Sigma公司。
, 百拇医药
统计学方法 结果以
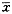 ±s表示,组间资料用t检验进行统计学处理。
±s表示,组间资料用t检验进行统计学处理。2 结果
急性心肌梗塞对红细胞3H-L-Arg转运的影响:红细胞L-Arg主要由Y+载体转运,少量由Y+L载体转运。急性心肌梗塞组的总转运速率在不同浓度底物L-Arg时均较正常对照组降低(P<0.01),其中主要为Y+载体转运速率下降(P<0.01),而Y+L载体在正常对照组及急性心肌梗塞组均无明显变化(P>0.05,附图)。Eadie-Hofstee Plot分析:两组的总转运、Y+转运、Y+L转运均呈高亲和特征。急性心肌梗塞组总转运及Y+载体的最大转运速率(Vmax)分别较正常对照组降低14%(P<0.05)及18%(P<0.01),米氏常数(Km)增加32%及46%(P<0.01),而Y+L载体的Vmax及Km与正常对照组差异无显著性(P>0.05,表1)。

, 百拇医药
附图 急性心肌梗塞组和正常对照组红细胞左旋精氨酸转运饱和曲线
表1 2组患者红细胞左旋精氨酸最大转运速率和米氏常数比较(
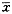 ±s) 组别
±s) 组别例数
最大转运速率[nmol/(107 cells.min)]
米氏常数(μmol/L)
总内流
Y+载体
Y+L载体
, 百拇医药
总内流
Y+载体
Y+L载体
正常对照组
10
5.27±0.40
4.35±0.32
0.98±0.06
31.7±4.0
33.3±2.9
27.7±3.3
急性心肌梗塞组
, http://www.100md.com
14
4.52±0.32*
3.58±0.26**
0.97±0.06
41.8±3.2**
48.5±4.2**
26.9±2.6
注:与正常对照组比*P<0.05 **P<0.01
急性心肌梗塞对红细胞NOS含量、NOS活性及cGMP含量的影响:急性心肌梗塞组患者红细胞NOS含量及NOS活性分别较正常对照组降低13%(P<0.05)及44%(P<0.01);cGMP含量较正常对照组下降27%(P<0.05,表2)。
, 百拇医药
表2 2组患者红细胞内一氧化氮合酶含量、活性及环磷酸鸟苷含量比较(
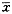 ±s) 组别
±s) 组别例数
一氧化氮合酶含量
(mg/5×107 cells)
一氧化氮合酶活性
(pmol/mg.min)
环磷酸鸟苷含量
(pmol/5×107 RBC)
正常对照组
, 百拇医药
10
0.52±0.06
22.51±3.26
0.22±0.02
急性心肌梗塞组
14
0.45±0.03*
12.71±2.21**
0.16±0.02*
注:与正常对照组比*P<0.05 **P<0.01
, 百拇医药
3 讨论
急性心肌梗塞主要病因是冠状动脉内血栓形成,已知内皮及血小板NO生成减少可促进血栓形成,可能是急性心肌梗塞的发病环节之一[1]。近年发现不仅血小板和内皮细胞中存在L-Arg-NO途径,红细胞也存在L-Arg-NO途径:即血浆中的NO合成的底物L-Arg经Na+—非依赖性高亲和Y+载体和Y+L载体转运入红细胞[4],在红细胞内存在的内皮型一氧化氮合酶(eNOS)作用下,生成NO,并持续、小量地释放入血,通过细胞的第二信使cGMP发生抑制血小板凝集、调节血管张力、减轻缺血再灌注损伤等心血管保护作用[2]。但急性心肌梗塞时红细胞L-Arg-NO途径是否发生变化尚未见报道。
本工作观察到红细胞L-Arg的跨膜转运主要由Y+载体介导,少量由Y+L载体介导,与文献报道一致[4]。急性心肌梗塞时转运方式无改变,但Y+载体的Vmax较正常对照组降低,Km增加,提示参与转运的载体数量减少且与L-Arg的亲和力下降;而Y+L载体无明显变化。所以急性心肌梗塞时红细胞L-Arg的总转运能力是下降的。
, 百拇医药
除L-Arg的跨膜转运外,NOS是NO生成过程的另一重要限速步骤。本研究结果发现急性心肌梗塞患者红细胞内NOS含量及NOS活性均较正常对照组降低。cGMP是NO的下游分子,红细胞内cGMP的含量与内源性NO生成量一致[6],测定cGMP的含量可以间接反映NO的生成量。结果显示急性心肌梗塞组患者红细胞cGMP的含量较正常对照组下降,提示NO生成减少。NO的减少可增加血小板的高反应性,促进血栓形成,增加血管张力,可能会在一定程度上加速急性心肌梗塞的进程,加重心肌缺血—再灌注损伤,促进溶栓后血管再闭塞或再次心肌梗塞。
本研究结果表明,急性心肌梗塞患者红细胞存在L-Arg-NO途径的多环节功能障碍,最终使NO生成减少,可能会加重或促进血栓的形成,提示临床上需加强急性心肌梗塞后抗凝、抗血小板治疗;也支持应用硝酸酯类等NO供体,以迅速、有效地补充NO,不仅能扩张冠状动脉、增加冠状动脉血流,也能防止血小板粘附、聚集。由于L-Arg转运具饱和性质,补充L-Arg等NO前体时需考虑其生物利用度。急性心肌梗塞患者红细胞L-Arg-NO途径异常的发生机制尚不清楚,需进行深入研究。
, http://www.100md.com
作者简介:王晓阳(1965-)女,主治医师 硕士研究 生 主要从事心血管临床工作
参考文献
1,Freedman JE,Ting B,Hankin B,et al.Impaired platelet production of nitric oxide predicts presence of acute coronary syndromes.Circulation,1998,98:1481—1486.
2,Chen LY,Mehta JL.Evidence for the presence of L-arginine-nitric oxide pathway in human red blood cells:relevance in the effects of red blood cells on platelet function.J Cardiovasc Pharmacol,1998,32:57—61.
, 百拇医药
3,Deliconstantions G,Villiotou V,Stavrides JC,et al.Nitric oxide and peroxynitrite production by human erythrocytes:a causative factor of toxic anemia in breast cancer patients.Anticancer Res,1995,15:1435—1446.
4,Ribeiro ACM,Hanssen H,Kiessling K,et al.Transport of L-arginine and the nitric oxide inhibitor NG-monomethyl-L-arginine in human erythrocytes in chronic renal failure.Clin Sci,1997,93:57—64.
5,Deves R,Angelo S,Chavez P.N-Ethylmaleimide discriminates between two lysine transport systems in human erythrocytes.J Physiol,1993,468:753—766.
6,Ghigo D,Todde R,Ginsburg H,et al.Erythrocyte stages of Plasmodium falciparum exhibit a high nitric oxide synthase (NOS) activity and release an NOS-inducing soluble factor.J Exp Med,1995,182:677—688.
收稿:1999-09-06
修回:2000-01-26, 百拇医药