制药企业GMP文件生命周期管理调查Δ
培训,1GMP文件生命周期管理模型简介,2对象与方法,1调查目的,2调查对象,3调查方法,3制药企业GMP文件生命周期管理中存在的问题,1文件起草缺乏系统性,完整性,可操作性及扩展性,2文件审核形式化,3对相关人员的培训效
丁 静(浙江医药高等专科学校,浙江宁波 315100)据国家食品药品监督管理总局(CFDA)统计,截至2013年7月,我国通过2011年版《药品生产质量管理规范》(GMP)认证的无菌药品生产企业仅占25.9%,非无菌药品生产企业仅占13.4%[1]。可见,我国制药企业GMP整体认证通过率较低,认证压力较大。国家食品药品监督管理部门曾明确规定,全国所有无菌药品生产企业应在2013年12月31日前达到2010年版GMP认证要求,而非无菌药品生产企业应在2015年12月31日前达到2010年版GMP认证要求。届时,那些未通过2010年版GMP认证的企业,将一律被要求停产,而先行通过2010年版GMP认证的企业可获得多方面扶持。因此,所有制药企业都应当抓住有利时机,积极应对挑战,除开展硬件设施方面的改造外,还应建立一套系统、科学、实用的文件管理系统,并持续、有效地开展GMP文件生命周期管理,以顺利通过2010年版GMP认证。本文拟就如何进行GMP文件生命周期管理以符合2010年版GMP要求等问题进行探讨和分析。
1 GMP文件生命周期管理模型简介
“文件生命周期”这一概念最早由美国档案学者菲利普・布鲁克斯提出。文件生命周期理论是指文件从产生直至因丧失作用被销毁或因具有长远历史价值被档案馆永久保存的整体运动过程[2]。该理论为文件的全过程管理奠定了理论基础,GMP文件管理在一定程度上体现了该理论的思想。但是,由于该理论主要是针对档案馆的文件管理,因此并不完全适用于制药企业的GMP文件管理。为此,笔者在该理论的基础上,结合GMP文件管理的特殊性,提出了GMP文件生命周期管理模型(见图1)。该模型覆盖了GMP文件整个生命运动的过程和形态,体现了文件的生命是“往复运动于起草到处置的连续的过程”,反映了GMP文件从起草、审核、批准、分发、培训、生效、执行、保管、复审、变更、替换、撤销、销毁等完整的运动过程,强调GMP文件的整体性、系统性、连贯性和运动性。该模型对指导和解释我国制药企业文件管理中的一些实际问题具有重要的现实意义。开展GMP文件生命周期管理对提升制药企业的质量管理水平、促进GMP的有效实施和推动我国制药工业持续健康发展具有举足轻重的作用。
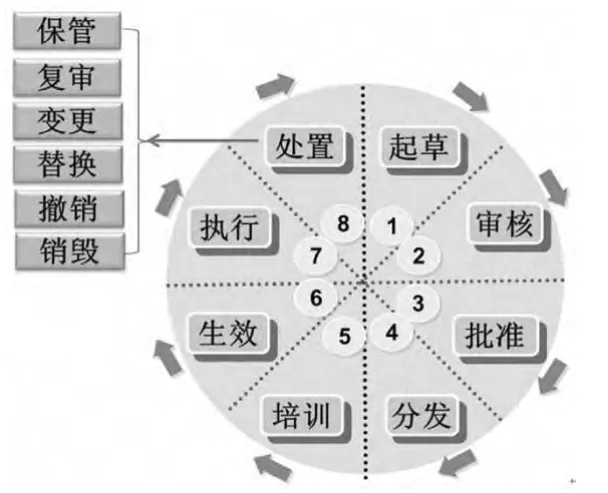
图1 GMP文件生命周期管理模型Fig 1 GMPdocument lifecycle management model ......
您现在查看是摘要页,全文长 12807 字符。