临床试验项目准备及启动阶段的时间管理(2)
3 伦理上会阶段伦理上会审批时间长是很多研究中心滞后临床研究的重要方面之一[9]。上会资料除了常规的研究方案,研究者手册,知情同意书,CRF表,招募广告,企业三证等之外,各中心也会有一些细微差别,如装订份数、PPT要求等方面。由于各家医院伦理上会时间不同,需要项目经理(PM)收集和整理一份详尽的实时更新的上会时间表,以便通过督促临床监查员(CRA)来控制伦理资料准备、伦理资料递交、伦理费用支付等一系列环节。在方案定稿阶段,开始机构立项准备工作,这里就运用了快速跟进的方法,可以部分解决首家伦理上会中心即组长单位及时上会的问题。项目经理要经常审查进度数据,通过关键路径来管理项目进度。图2展示了一个常规伦理上会过程。
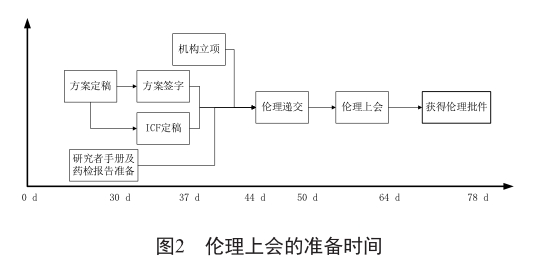
4 协议签署阶段
完成与研究机构完成合同的签署代表着项目已经进入到启动阶段,每家机构签署合同时间快慢不同,一般需要2个月左右时间。PMBOK中早期规划、掌握资源信息具有重要价值,具体来说从中心调研开始 ......
您现在查看是摘要页,全文长 4602 字符。