重组单克隆抗体的纯化研究
层析,培养液,填料,1细胞培养液澄清,2抗体捕获,3抗体精制纯化,4病毒灭活,5纯化工艺放大
邹有土・质量控制・
重组单克隆抗体的纯化研究
邹有土
重组单克隆抗体是新一代生物工程技术产品,其通过特定的靶点发挥药效[1]。随着大规模哺乳动物细胞培养技术的发展,工业化细胞培养液体积可达 1 万升以上,抗体表达量可达 5 g/L 以上,极大地加重了重组单抗下游纯化的压力[2-3],下游纯化成为限制重组单抗工业化扩大的主要因素[4-6]。重组单抗杂质控制浓度指标见表 1,这些指标必须通过离心、过滤和色谱层析纯化后控制在一定浓度以下[7-10]。重组抗体的纯化一般可以分为细胞培养液澄清、抗体捕获、抗体精制纯化、病毒灭活和纯化工艺的放大等流程。

表1 重组单抗杂质控制浓度以及去除方法
1 细胞培养液澄清
在细胞培养过程中,在重组单抗分泌到培养液的同时,培养液中也含有大量的细胞颗粒、碎片、细胞器及细胞DNA[11]。工业化规模的细胞培养液澄清通常由三个步骤完成,具体步骤见图 1[12]。第一步处理通常设置为离心,培养液中的细胞和细胞碎片通过离心去除后可大大减轻后续深层过滤或者微滤步骤的负荷。离心操作可分为批处理模式和连续流模式。批处理模式适用于实验室规模,而连续流模式可以处理更大的培养液体积,更适用于工业化规模。随着低离心剪切力离心机的发展,离心、过滤的混合型离心机在细胞澄清步骤的应用已经越来越广泛[7]。在细胞培养液中加入一定的絮凝剂,可以使细胞悬浮物如细胞碎片等更易离心去除,进一步改善细胞培养液的澄清度,减少深层过滤的步骤。而微滤在细胞培养液澄清中,其效果要好于离心机,且其成本较低,但微滤会扩大料液体积 3 ~ 4 倍,导致后续纯化负担增加,不利于工业化生产[4]。
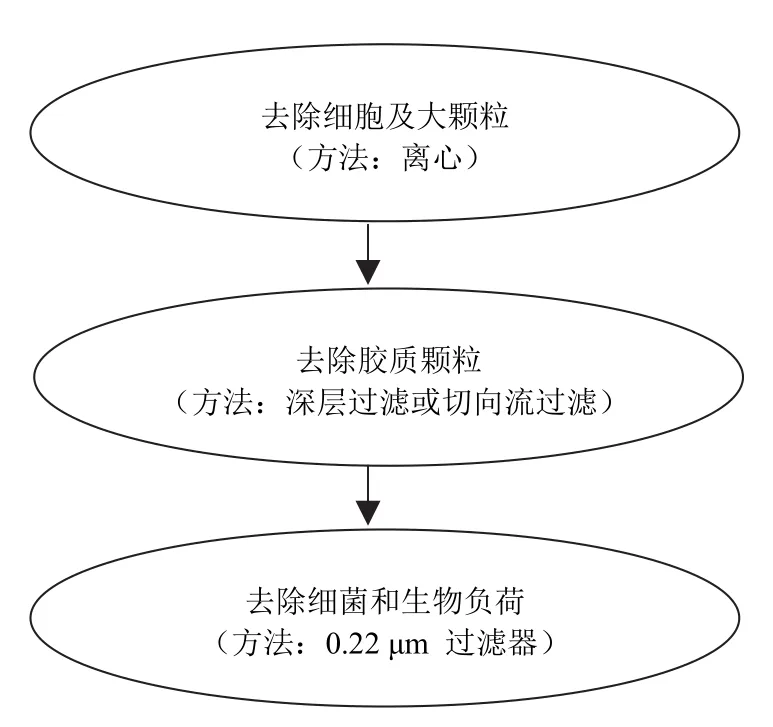
图1 细胞培养液澄清三步骤
深层过滤和切向流过滤通常在澄清过程的第二步使用。对于大规模纯化,深层过滤处理的体积相对比较小,而切向流过滤则具有更大的处理能力,并兼具浓缩的功能。但深层过滤使用方便、清洁、高效,在重组单抗的工业纯化中应用广泛。深层过滤属于非均相分离,能够使料液通过整个多孔介质而不仅仅是表面过滤 ......
您现在查看是摘要页,全文长 13287 字符。